
| Avant la vie...Propriétés des molécules organiquesLes molécules organiques ne s'associent pas en n'importe quel endroit de leur structure, elles possèdent des groupements d'atomes plus réactifs que d'autres où l'association aura lieu. Donc les associations ne sont pas totalement dues au hasard mais sont "dirigées" en fonction de la présence ou non de tels sites réactifs. Quand deux acides aminés se rencontrent au hasard, l'extrémité la plus "acide" (en rouge) d'un des acides aminés va s'associer à l'extrémité la plus "basique" de l'autre molécule (en bleu), avec une libération d'eau. 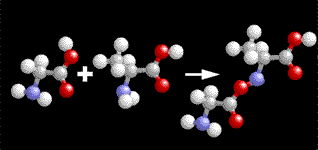 C'est ce que l'on appelle une liaison peptidique. Cette liaison est à l'origine de la formation de très grosses molécules, les protéines, par chaînage de différents acides aminés à la suite les uns des autres. Dans la soupe primitive, les protéines ne pouvaient pas être formées en raison de l'absence d'enzymes suffisamment élaborées, mais de petits peptides ont pu se former de cette façon sous l'influence de fortes températures. Ces longues molécules se replient dans les trois dimensions, par regroupement d'acides aminés distants, en fonction d'affinités interne. La configuration 3D des protéines leur a apporté une stabilité plus grande, mais a également permit l'apparition de nouveaux sites réactifs par rapprochement de 2 séquences d'acides aminés qui étaient jusqu'alors séparées. Ainsi certaines protéines ont eu une activité catalytique sur d'autres molécules, ce sont les enzymes. Elles permettent de découper, coller, modifier les molécules sur lesquelles elles agissent. La stabilité des molécules permet une
meilleure résistance aux conditions environnantes. De
même la forte synthèse d'une molécule
permet de contrecarrer son taux de destruction. Donc les
réactions de catalyse
en chaîne ou d'autocatalyse permettent une meilleure
stabilité. |